研究紹介
山本研究室で,これまでに開発した分子イメージング機器の一部を紹介致します。これら以外にもさまざまな機器を開発してきました。また現在も,世界初の分子イメージング装置を複数開発中ですので,今後完成しましたら,ここで紹介していく予定です。
超高分解能PET装置の開発
PETは,生体中分子の分布などを測定するための撮像装置であり,分子イメージング研究における中核機器として注目されてきました。生体内に目印となる放射性物質を投与し,それが放出する陽電子(ポジトロン)が体内の電子と結合した時に放出される消滅放射線をコンピューター処理することで,生体分子の分布や濃度を測定することができます。これまで開発されてきたPETの空間分解能は技術的な問題から1.5mm程度でしたが,マウスなどの小動物の撮像を精度撮像できないという問題点がありました。
山本研究室では,今回0.5mmのシンチレータ(放射線を検出し,光を発する材料),独自のライトガイド(シンチレータから出た光の通り道を変える材料),新型光センサー:Si-PMアレーを用いて高い空間分解能を実現できる放射線検出器を開発しました。その結果,0.7mmの空間分解能を実現しました。この値は現状,世界最高となります。
発表論文:Yamamoto S, Watabe H, Kanai Y, Watabe T, Kato K, Hatazawa J. Development of an ultrahigh resolution Si-PM based PET system for small animals. Phys Med Biol. 2013 Nov 7;58(21):7875-88

開発した超高分解能PET装置の検出器リング(左)とマウス撮像中の写真
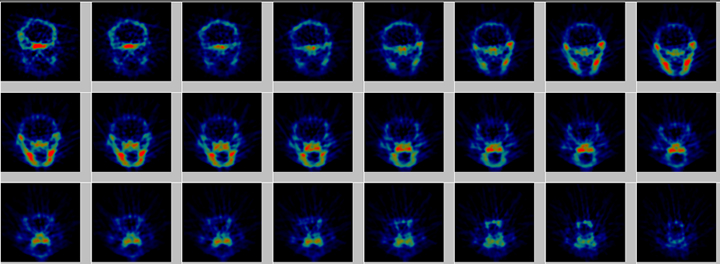
超高分解能PET装置で撮像したマウスの頭部画像
ウエアラブルPET装置:PET-Hatの開発
ヒトの頭部のPET撮像においては,通常寝たままの状態で,頭部を固定して撮像します。しかし,そのような状態では繊細な刺激に対する脳の反応を計測することは困難です。座ったままで被験者にある程度の動くことができれば,より自然な状態でのPET測定が可能となります。そこで装着型PET装置:PET-Hat開発の開発を行いました。
開発した装置は,検出器リングが3方向に自由に動くことができ,被験者の動きをPET装置の検出器リングが追従して動く機構を世界で初めて実現しました。また被験者は座ったままで撮像可能となりました。PETを使った脳の機能測定に威力を発揮することが期待されます。
発表論文:S. Yamamoto, M. Honda, T. Oohashi, K. Shimizu, M. Senda, Development of a Brain PET System, PET-Hat: A Wearable PET System for Brain Research, IEEE Trans. Nucl. Sci., vol. 58, no. 3, pp. 668-673, 2011

座位で測定可能なウエアラブルPET装置の写真

動いている被験者のビデオ画像の一部
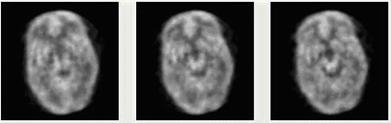
PET-Hatで撮像したヒト脳ファントムの画像
PET/MRI一体型装置の開発
PETとMRIの同時測定が可能なPET/MRI装置は,新しい分子イメージング機器として注目されています。PETは高い感度でポジトロン放出核種で標識した分子プローブの分布を測定可能です。一方,MRIは種々のコントラストで,高い空間分解能の解剖学的画像を得ることができる長所があります。この2つの代表的な分子イメージング機器を一体化することで,PETとMRIを同時に撮像可能となり,測定時間の短縮,位置合わせの精度の向上など,多くの利点が生まれます。山本研究室では世界に先駆けPET/MRI一体型装置の開発を行い,多くの成果を上げています。
PETとMRIの一体化行う場合の最も大きな問題点は,PETとMRIが相互に影響を与え,撮像ができなくなったり画質が劣化する点があげられます。PET装置の一般的な光センサーである光電子増倍管(PMT)はMRIの静磁場中では電子軌道が大きく影響を受け,通常は使用できませんので,新しい概念のPET装置が求められることになります。
山本研究室では,光ファイバーが磁場の影響を受けないことを利用し,PETのシンチレータと光センサーの間に光ファイバーを用いることで相互影響の無いPET/MRI一体型装置を実現しました。この開発により,MRIとPETの同時測定が可能となりました。このPET/MRI一体型装置のPETの空間分解能は1.2mmで,PET/MRI一体型装置としては世界最高です。
発表論文:S. Yamamoto, H. Watabe, Y. Kanai, T. Watabe, M. Aoki, E. Sugiyama, K. Kato, J. Hatazawa. Development of a flexible optical fiber based high resolution integrated PET/MRI system, Med. Phys., 39(11), pp. 6660-6671, 2012

PET/MRIに用いた光ファイバー型PET用検出器(左)と一体型装置(右)
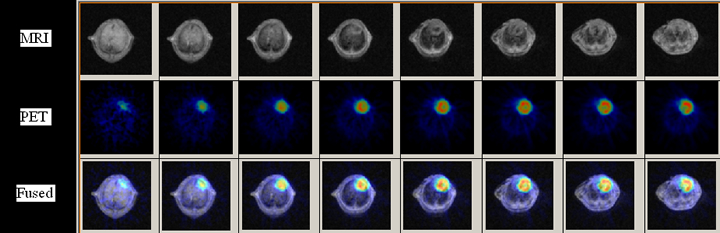
PET/MRI一体型装置で撮像したマウスの胸部画像:上からMRI,PET,融合画像
高分解能ガンマカメラの開発
ガンマカメラやSPECT装置は,比較的容易に放射性核種を使えるため,分子イメージングの分野で注目されています。しかし高い分解能を得ることが難しく,高分解能の画像を得ることがこれまで出来ないという問題点がありました。山本研究室では,小さなシンチレータを束ねたブロックを位置検出型光電子増倍管に光学結合し,タングステンコリメータを組み合わせることで1mm以下の高分解能のガンマカメラ装置を開発し,極めて鮮明なラットの画像を得ることに成功しました。
発表論文:Yamamoto S, Watabe H, Kanai Y, Kato K, Hatazawa J. Development of a high-resolution YSO gamma camera system that employs 0.8-mm pixels. Ann Nucl Med. 2014(in-press)

開発したガンマカメラ(左),ファントム画像(中),USBメモリーの透過画像
 開発した高分解能ガンマカメラで撮像したラットの全身画像
開発した高分解能ガンマカメラで撮像したラットの全身画像
高分解能α線カメラの開発
高分解能α線カメラは,α線放出核種内服療法の基礎研究のためのオートラジオグラフィやプルトニウム粒子の検出などに重要です。当研究室ではα線放出核種の分布を画像化する装置を開発しています。
本研究室の博士後期課程1年森下さんらは,高分解能α線カメラの開発に成功し,Nuclear Instruments and Methods in Physics Research Section A 誌に成果を発表しました。このα線カメラはシリコンフォトマル(Si-PM)アレーと0.1mm厚のGAGG結晶を光学結合し,α線のみを選択的に高分解能で画像化したというものです。シリコンフォトマル(Si-PM)アレーを用いたα線カメラの開発に関する報告は世界で初めてとなります。この研究は北海道大学と原子力研究機構との共同研究として進められました。
発表論文:Y. Morishita, S. Yamamoto, K. Izaki, J. H. Kaneko, K. Toui, and Y. Tsubota. Development of a Si-PM based alpha camera for plutonium detection in nuclear fuel facilities. Nuclear Instruments and Methods in Physics Research Section A , 2014 (in-press)

0.1mm厚のGAGG結晶 Si-PMアレー α線カメラ
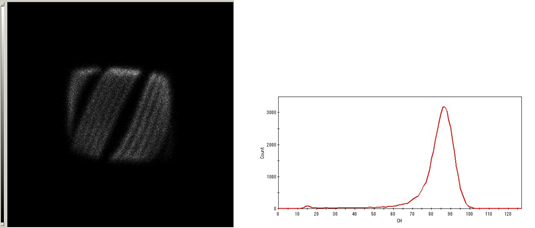
スリットファントム画像(0.4mmスリットが分解) 5.5MeVα線エネルギースペクトル
GAGG高感度低バックグランド放射性セシウムモニターの開発
放射性セシウムを含む食品の汚染検査には高エネルギーガンマ線(137Cs:662keV、134Cs:605keVと794keV)を検出する方法が用いられます。しかし高エネルギーガンマ線を検出する方法は,環境中の40Kなどからのガンマ線の散乱成分などがバックグランド計数となり,検出限界を下げることが困難であることが問題となっています。この問題点を解決するために137Csあるいは134Csから放出される~32keVのX線を検出することで,バックグランド計数を減少させ,検出限界を下げるという新しい方法の放射性セシウム井戸型検出器を開発し,性能を評価しました。検出器には1mm厚のGAGGを,ライトガイドを介して4個被検体周辺に,1個直接光電子増倍管(PMT)に光学結合することで井戸型検出器を構成し,高感度を達成しました。開発した装置はバックグランドが低く,10ccという少ない試料で,1000秒測定で100Bq/kgの放射性セシウム濃度まで測定可能であることが明らかになりました。今後メーカーによる製品化が期待されます。
発表論文: S. Yamamoto and Y. Ogata, A compact and high efficiency GAGG well counter for radiocesium concentration measurements. Nuclear Instruments and Methods in Physics Research Section A , 2014 (in-press)

ライトガイドとGAGGシンチレータ(左), 井戸型検出器(中), 井戸型検出器システム(右)
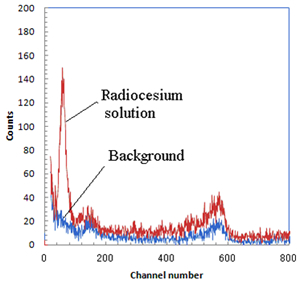
放射性セシウム(137Cs: ~9Bq)溶液とバックグランドのエネルギースペクトル
PETの原理を用いた低バックグランド高感度放射性セシウム測定装置の開発
東京電力福島第一原子力発電所事故により環境中に放出された放射性物質による環境汚染が大きな問題となっていいます。特に長半減期である放射性セシウムの自然生態系への取り込みは極めて深刻であり,食品などを低バックグランドで計測する手法が切望されています。低バックグランド測定が困難な理由は、環境中の主に40Kからの高エネルギーガンマ線が検出されるためで、バックグランド計数を減らすためには、厚いガンマ線シールドが必要になり、検出装置が大きく、また重くなる問題点がありました。本研究室では134Csからの605keVと796keVガンマ線が同時に放出されることを利用し, PETのデータ収集電子回路を用いて同時計数することで超低バックグランド放射性セシウムの検出を可能にしました。
ゲルマニウム酸ビスマス(BGO)をを光電子増倍管に光学結合した検出器4個を層とし,放射性セシウム検体の周りに2層配置した検出器を開発し,PET装置の回路を用いて同時計数を行いました。その結果,単一光子放出核種を計測したところ、同時計数することでカウントを0.11%に減らすことができました。またバックグランド計数を測定したところ、同時計数により0.52%に減らすことができました。134Csに対する感度は平均で12%でした。開発した装置の、10分間測定における放射性セシウムに対する検出下限放射能濃度は9.2Bq/kgと国の定める放射性セシウム食品モニターの基準(50Bq/kg)より十分に小さいという有望な結果が得られました。このの方式による放射性セシウム測定装置は、厚いガンマ線シールドを必要とせず、検出装置の大きさも比較的小さく、また重量も軽くできる有望な測定法であることが明らかになりました。
発表論文:Yamamoto S, Ogata Y. Low background high efficiency radiocesium detection system based on positron emission tomography technology. Rev Sci Instrum. 2013 ;84(9):093507

開発した低バックグランド高感度放射性セシウム測定装置の概念図(左)と写真(右)
PET/チェレンコフ光同時撮像装置の開発
チェレンコフ光撮像法は原理的にポジトロン核種の分布を極めて高い空間分解能で計測することが可能です。しかし、この撮像法は,動物実験等の測定においては、生体内部から発する多重散乱された光を検出することになり画質が劣化するため,分子イメージング研究における有用性は未だ不明なままです。今回,世界で初めて対向型PET/チェレンコフ光一体型撮像装置を開発し,対向型PET装置による画像とチェレンコフ光画像の同時測定を可能にしました。
図1(左)にPET/チェレンコフ光同時撮像装置の概念図を示します。消滅放射線同時計測によるポジトロン核種画像とチェレンコフ光画像の同時撮像を実現するために、対向型PETの側面の空間を利用して、チェレンコフ光撮像のための、電子増倍型CCD(EM-CCD)カメラを配置しました。被検体の上方にミラーを傾けて配置し、上方に出射したチェレンコフ光を側面方向から撮像可能となりました。開発した装置の写真を図1(右)に示します。
開発したPET/チェレンコフ光複合画像化装置で同時測定して得られたF-18-FDG(最大陽電子エネルギー: 0.64 MeV)投与ラット画像を図2に示します。PET画像はハーダー線への集積が,チェレンコフ光画像は眼球での発光が観察され,各モーダリティーで異なる位置に検出されるという興味深い結果が得られました。
発表論文:Yamamoto S, Hamamura F, Watabe T, Ikeda H, Kanai Y, Watabe H, Kato K, Ogata Y, Hatazawa J. Development of a PET/Cerenkov-light hybrid imaging system. Med Phys. 2014 Sep;41(9):092504.
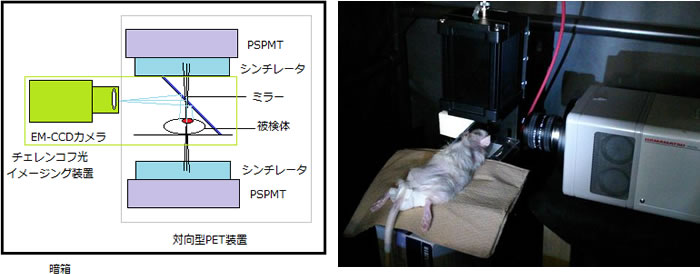
図1 PET/チェレンコフ光同時撮像装置の概念図(左)と開発した同時撮像装置(右)
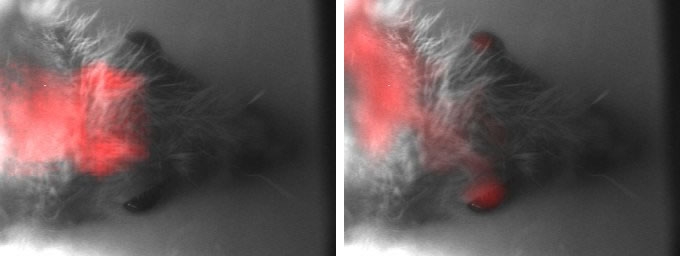
図2 PET/チェレンコフ光同時撮像装置で撮像のしたPET画像と光学画像の融合画像(左)と
チェレンコフ画像と光学画像の融合画像(右):分布の違いが明らかになった。
陽子線照射中に生成する陽電子分布のチェレンコフ光計測による画像化
陽子線治療(図1)は,陽子線が選択的に高線量を腫瘍に与えることが可能なため注目を集めています。陽子線治療においては,間違いなく陽子線が目的とする部位に照射されていることを確認するために,照射中あるいは照射直後に線量を測定したいという要求があります。現在は,陽電子放射型断層撮像法(PET)を用いて,陽子線照射により生じた陽電子を画像化することで線量分布をえることが試みられていますが,PET装置は空間分解能が比較的低い(4-5mm程度)ことやコストが高い(数億円)という問題点がありました。
陽電子が物質中を運動するときに,チェレンコフ光という微弱な光を放出することに着目;この光を高感度CCDカメラで撮像することで,これまでにない0.7mmという極めて高い空間分解能で画像化することに今回,陽子線治療センターと共同で,世界で初めて成功しました。アクリル製のファントムにエネルギーの異なる陽子線を照射し,生成した陽電子の分布をCCDカメラで撮像しました。その結果,陽電子の分布を明確に高い空間分解能で得ることができました。(図2)。測定した画像から得られた陽電子の分布は,コンピュータシミュレーションの結果とも良く一致しました。
発表論文:S. Yamamoto, T. Toshito, K. Fujii, Y. Morishita, S. Okumura, M. Komori, High resolution Cerenkov light imaging of induced positron distribution in proton therapy. Med. Phys. 41, 111913, 2014
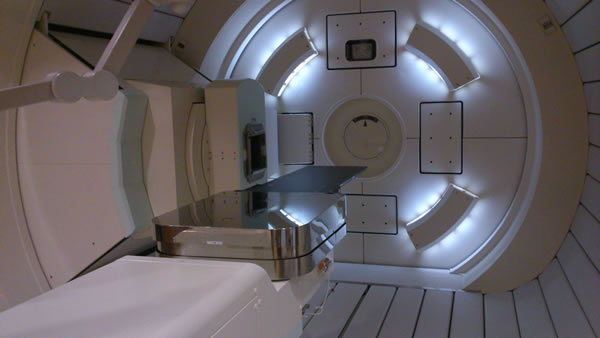
図1 陽子線治療装置(名古屋陽子線治療センターの照射装置)

図2 今回の研究で得られた105.9MeV(左)と
221.4MeV(右)の陽子線照射で生じた陽電子の分布画像(オレンジ色)。
白黒の四角い部分がアクリルファントム
陽子線照射中に生成する陽電子分布のガンマカメラによる画像化
陽子線治療においては,間違いなく陽子線が目的とする部位に照射されていることを確認するために,照射中あるいは照射直後に線量を測定したいという要求があります。現在は,陽電子放射型断層撮像法(PET)を用いて,陽子線照射により生じた陽電子を画像化することで線量分布を得ることが試みられていますが,PET装置は被検体を囲む必要がある上,コストが高いという問題点があります。
陽電子が電子と結合した後,放出する消滅放射線(511keVガンマ線)は高エネルギーガンマカメラで撮像できる可能性があります。そこで高エネルギーガンマカメラを開発し,名古屋陽子線治療センターにおいて,陽子線照射によりファントム中の生成する陽電子分布の画像化を試みました(図1)。その結果,ファントム中の陽電子の分布を明確に得ることができることが明らかになりました(図2)。本研究では,比較的廉価なガンマカメラを用いて陽子線照射時の線量分布を画像化できる可能性があることを実証しました。被検体から離れた一方向から簡単に画像化できるという利点もあり,将来の応用が期待されます。本研究は名古屋陽子線治療センター,原子力研究機構との共同研究として行われました。
発表論文:S. Yamamoto , T. Toshito, M. Komori, Y. Morishita, S. Okumura, M. Yamaguchi, Y. Saito, N. Kawachi, S. Fujimaki. Monitoring of positron using high-energy gamma camera for proton therapy. Ann Nucl Med. Apr;29(3):268-75, 2015
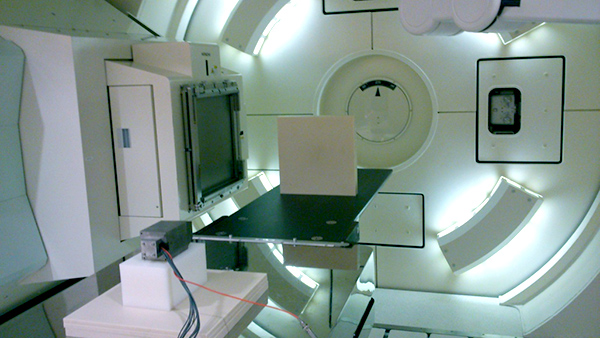
図1 陽子線治療装置を用いた高エネルギーガンマカメラによる
陽子線照射生成ポジトロン画像化の実験風景:
左から陽子線がファントム(中央の四角い物体)に照射される。

図2 高エネルギーガンマカメラで撮像した129MeV(左)と
221MeV(右)の陽子線照射で生じた陽電子の分布画像(オレンジ色)を
光学画像(緑色)と融合した画像。エネルギーの高い陽子線が
ファントム中の深い場所まで到達していることが分かる。
陽子線照射により生じる微弱光画像から、陽子線の飛程を高精度で計測
陽子線治療は、陽子線が選択的に高線量を腫瘍に与えることが可能なため、注目を集めています。陽子線治療においては、間違いなく陽子線が目的とする部位に照射されていることを確認するために、照射中あるいは照射直後に線量を測定したいという要求があります。現在は、陽電子放射型断層撮像法(PET)を用いて、陽子線照射により生じた陽電子を、照射後に画像化することで線量分布を得ることが試みられていますが、PET装置は空間分解能が比較的低い(4-5mm程度)ことやコストが高い(数億円)上、照射中の線量分布と、発生する陽電子の分布が異なるという問題点がありました。また、陽子線照射中に線量を知ることができない問題点もありました。一方で、陽子線照射により、水が発光するとは考えられていなかったことから、これまで陽子線照射中の線量分布画像を光計測で得たという報告はありませんでした。
今回、世界で初めて、陽子線が水中で微弱光を発することを発見し、この微弱光を高感度CCDカメラで撮像することで陽子線が水に与える線量分布を画像化することに成功しました。容器に封入した水に陽子線を照射した状態で、高感度CCDカメラで容器中の水を撮像しました。その結果、陽子線によって水に生じる微弱光の分布を鮮明に画像化することができました。(図-1(A))。また、画像から得られた陽子線の飛程の形状は、明確なブラッグピークを有し、その飛程は電離箱を用いた測定値と一致しました(図1(B))。今回の研究成果は、新しい陽子線計測法の発見といえるものであります。検出した微弱光は陽子線照射で水に生じたフリーラジカルに起因すると考えています。
水は、人体を模擬する最良の物質でありますが、今回の研究は、水そのものが陽子線の検出器となりうる性質をもっていることを明らかにしました。今回実験に用いた手法は、陽子線照射中に実時間で線量分布の画像化が可能であり、高い空間分解能の画像が得られることから、陽子線治療における線量評価や装置の精度管理に大きく貢献するものと期待されます。
本研究は、名古屋陽子線治療センターとの共同研究として行われました。
発表論文:Seiichi Yamamoto, Toshiyuki Toshito, Satoshi Okumura, and Masataka Komori, Luminescence imaging of water during proton-beam irradiation for range estimation, Medical Physics, 42 (11), 6498-6506, 2015
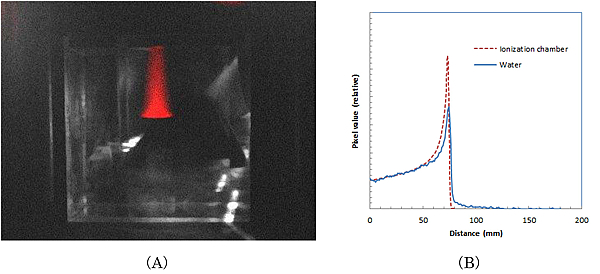
図1 今回の研究で得られた水に100.2MeV(左)の陽子線を照射したときの線量分布画像(オレンジ色の部分)(A)と画像から得られた線量分布のプロファイル(B)
